Бролуцизумаб vs Афлиберцепт при неоваскулярной форме возрастной макулярной дегенерации
Інші публікації цього автора
Jaffe G.J.
Інші публікації цього автора
Sallstig P.
Інші публікації цього автора
Адаптированный перевод: к.м.н. Палёха О.Н., медицинский центр АЙЛАЗ
Бролуцизумаб vs Афлиберцепт при неоваскулярной форме возрастной макулярной дегенерации
Интравитреальные анти-VEGF-инъекции представляют собой «золотой стандарт» терапии неоваскулярной формы возрастной макулярной дегенерации (Schmidt-Erfurth U. et al.).
Однако, соблюдение графика частых инъекций и частых повторных обследований довольно затруднительно для пожилых пациентов, их опекунов или помощников (Holz F.G. et al.).
Альтернативные варианты лечения с большими интервалами между инъекциями могли бы уменьшить нагрузку и способствовать лучшему комплайенсу.
Молекула бролуцизумаба (RTH258) – это гуманизированный одноцепочечный фрагмент антитела, способный связывать все изоформы VEGF-A. Бролуцизумаб обладает наименьшим молекулярным весом, составляющим 26 кДа, по сравнению с 115 кДа у афлиберцепта и 48 кДа у ранибизумаба (Gaudreault J. et al., Tietz J. et al.). Благодаря низкому молекулярному весу концентрация бролуцизумаба при его разведении может быть увеличена до 120 мг/мл, то есть при одной интравитреальной инъекции становится возможным ввести 6 мг бролуцизумаба в 0,05 мл раствора. По молекулярной массе 6 мг бролуцизумаба соответствуют примерно 12 дозам афлиберцепта (2 мг) и 22 дозам ранибизумаба (0,5 мг) (Tietz J. et al.).
Интравитреальное введение препарата в большей концентрации потенциально может сопровождаться большей продолжительностью его действия.
Цель – оценка эффективности и безопасности бролуцизумаба в сравнении с афлиберцептом.
Методы– группу афлиберцепта (Eyelea; Regeneron Pharmaceuticals Inc., Tarrytown, NY; 2,0 мг / 0,05 мл) составили 45 пациентов с неоваскулярной формой возрастной дегенерации макулы, а группу бролуцизумаба (Alcon Laboratories Inc., Fort Worth, TX; 6,0 мг / 0,05 мл) – 44 пациента. В каждой группе пациенты получили три загрузочные инъекции с интервалом в 1 месяц. Далее с 12-й по 32-ю неделю пациенты получали инъекции препаратов с интервалом в 8 недель. С 32-й по 56-ю неделю пациенты в группе афлиберцепта продолжали получать интравитреальные инъекции с интервалом в 8 недель (q8), а в группе бролуцизумаба плановые инъекции выполнялись с интервалом в 12 недель (q12). Пациентов наблюдали с интервалом в 4 недели, и при необходимости после согласования с пациентом, помимо плановых инъекций, им назначалось дополнительное введение препарата (режим лечения «по потребности»). Во время каждого визита проводилась оценка максимально корригированной остроты зрения и измерение толщины сетчатки в центральной зоне на снимках ОСТ.
На рисунке 1А продемонстрирована динамика изменения корригированной остроты зрения с начала лечения до 56 недели.
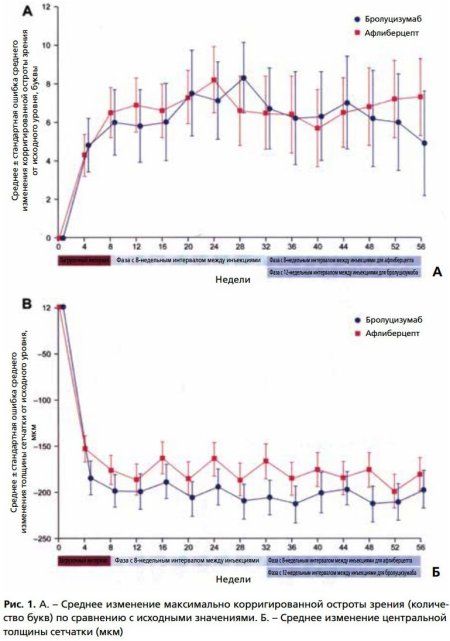
Рис. 1. А. – Среднее изменение максимально корригированной остроты зрения (количество букв) по сравнению с исходными значениями. Б. – Среднее изменение центральной толщины сетчатки (мкм)
В период «загрузочных доз» и в период с интервалом между инъекциями в 8 недель в обеих группах не было достоверных отличий в значении остроты зрения. К 12-й неделе после начала лечения прибавка в остроте зрения в группе бролуцизумаба составила 5,75 буквы, в группе афлиберцепта 6,89 буквы. К 40-й неделе после начала терапии прибавка в остроте зрения в группе бролуцизумаба составила 6,25 буквы, а в группе афлиберцепта – 5,75 буквы.
За первый интервал между инъекциями бролуцизумаба, составивший 12 недель (между 36-й и 44-й неделей после инъекции на 32-й неделе), статистически значимых изменений в остроте зрения в этой группе выявлено не было. За второй интервал между инъекциями бролуцизумаба, составивший 12 недель, произошло снижение зрения в среднем по группе на 1,3 буквы (между 48-й и 56-й неделей после инъекции на 44-й неделе).
В период с 32-й по 56-ю неделю (фаза q12) 10 пациентов получили дополнительные инъекции афлиберцепта и 14 пациентов – дополнительные инъекции бролуцизумаба в соответствующих группах. Семь пациентов с нестабильной остротой зрения в группе бролуцизумаба не получили дополнительных инъекций, и именно у них произошло снижение остроты зрения за 12-недельный интервал между последними инъекциями. У этих семи пациентов отмечался исходный слабый ответ на «загрузочные дозы» и сохранялась остаточная интраретинальная жидкость в течение всего периода наблюдения.
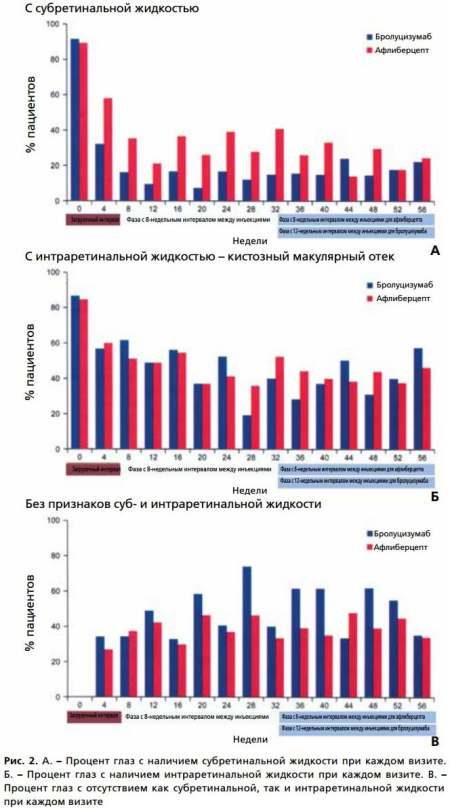
Рис. 2. А. – Процент глаз с наличием субретинальной жидкости при каждом визите. Б. – Процент глаз с наличием интраретинальной жидкости при каждом визите. В. – Процент глаз с отсутствием как субретинальной, так и интраретинальной жидкости при каждом визите
На рисунке 1Б представлена динамика изменения толщины сетчатки в центральной зоне за период с начала лечения до 56 недели. К 12-й неделе после начала лечения изменение центральной толщины сетчатки в группе бролуцизумаба составило 196,6 мкм, в группе афлиберцепта – 189,0 мкм, а к 40-й неделе после начала лечения – 197,5 и 178,3 мкм, соответственно.
На рисунке 2 представлена информация о количестве глаз с наличием суб- или интраретинальной жидкости. Субретинальная жидкость к 12-й неделе после начала лечения сохранялась у 9,3% и 20,9% пациентов в группах бролуцизумаба и афлиберцепта соответственно, а к 40-й неделе после начала лечения – у 14,6% и 32,5% пациентов соответственно. Интраретинальная жидкость к 12-й неделе после начала лечения сохранялась у 48,8% пациентов в обеих группах, а к 40-й неделе после начала лечения – у 36,6% и 40,0% пациентов в группах бролуцизумаба и афлиберцепта соответственно. Количество глаз без наличия суб- и интраретинальной жидкости к 12-й неделе после начала лечения составило 48,8% и 41,9% в группах бролуцизумаба и афлиберцепта соответственно, а к 40-й неделе после начала лечения – 61,0% и 35,0% соответственно.
Наиболее распространенным побочным эффектом интравитреального введения препаратов было конъюнктивальное кровоизлияние: 5 пациентов в группе бролуцизумаба и 7 пациентов в группе афлиберцепта. Другими побочными эффектами были плавающие мушки, снижение остроты зрения после инъекции и отслойка стекловидного тела.
Среди всех наблюдаемых пациентов за время лечения произошла одна смерть после третьей инъекции бролуцизумаба. Причиной смерти 80-летнего мужчины с анамнезом артериальной гипертензии, тромбоцитопении, спленомегалии, рака простаты и почек, стал инфаркт миокарда. У одного пациента из группы афлиберцепта произошла транзиторная ишемическая атака без летального исхода. По заключению экспертов, взаимосвязь между анти-VEGF-терапией и сосудистой катастрофой в обоих случаях исключить нельзя.
Данное исследование продемонстрировало не меньшую эффективность бролуцизумаба по сравнению с афлиберцептом. При режиме интравитреального введения каждые 8 недель оба препарата показали практически одинаковую прибавку в остроте зрения. При переходе на 12-недельный интервал между инъекциями острота зрения оставалась стабильной у 50% пациентов в группе бролуцизумаба. Снижение остроты зрения в среднем по группе произошло только за счет семи пациентов с исходным слабым ответом на лечение и нестабильной остротой зрения.
Возможно, в таких случаях показаны более частые инъекции препаратов.
При режиме интравитреального введения каждые 8 недель были выявлены определенные преимущества бролуцизумаба по сравнению с афлиберцептом:
ü оба препарата способствовали уменьшению центральной толщины сетчатки, но полная резорбция суб- и интраретинальной жидкости к 40-й неделе после начала лечения наблюдалась у 61,0% пациентов в группе бролуцизумаба и только у 35,0% пациентов в группе афлиберцепта;
ü безопасность бролуцизумаба, по данным авторов, сопоставима с безопасностью других анти-VEGF-препаратов;
Результаты проведенного исследования свидетельствуют о том, что бролуцизумаб, как минимум, не менее эффективен, чем афлиберцепт в режиме введения каждые 8 недель после трех ежемесячных загрузочных инъекций.
Кроме того, по результатам исследования можно предположить, что многим пациентам может подойти режим введения бролуцизумаба с интервалом в 12 недель после загрузочных инъекций. Режим лечения в каждом случае определяется индивидуально, базируясь на динамике изменения остроты зрения и центральной толщины сетчатки.
Dugel P.U., Jaffe G.J., Sallstig P. et al. Brolucizumab versus Aflibercept in participants with neovascular age-related macular degeneration: a randomized trial // Ophthalmology. – 2017. – Vol. 124, № 9. – P. 1296-1304.







Коментарі
Завантаження...