Неартифакический кистозный макулярный отёк
Главный редактор: Сэр Хемптон Рой, доктор медицины

Хотя наиболее частой причиной возникновения кистозного макулярного отёка (КМО) является синдром Ирвинга-Гасса после хирургии катаракты или другого хирургического вмешательства, заполненные жидкостью кистовидные полости в макуле могут возникать также на фоне других клинических причин. КМО часто является заключительным этапом многих внутриглазных заболеваний, в частности таких, которые затрагивают сосудистую систему глаза. Причины возникновения КМО могут различаться в небольшой степени в зависимости от этиологии, однако, она может также возникать как неспецифическое клиническое изменение. Если причина возникновения КМЭ не очевидна пациенту, необходимо провести детальную офтальмоскопию, а иногда и дополнительные исследования.
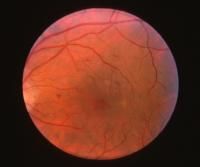
На рисунке показан кистозный макулярный отёк, возникший в результате непролиферативной диабетической ретинопатии. Фотография глазного дна с непролиферативной диабетической ретинопатией и явно выраженным макулярным отёком.
Патофизиология
Макулярный отёк характеризуется наличием избыточного количества жидкости внутри сетчатки, в отличие от скопления жидкости под или между слоями сетчатки (напр., отслойка нейроэпителия или серозная отслойка сетчатки). Количество жидкости, обычно присутствующее в сетчатке, регулируется в зависимости от осмотического и гидростатического давления между сетчаткой и сосудистой оболочкой, которые разделяет гемато-ретинальным барьером. Нарушение структуры этого барьера приводит к скоплению жидкости в кистоидных полостях самой сетчатки. Патология, связанная с нарушением структуры барьера, а также аномалии и разрушение клеток Мюллера могут быть причинами возникновения КМО.
В офтальмологии существует несколько версий относительно механизмов развития КМО. Характерное просачивание сквозь сосуды и отёк сетчатки лучше всего объясняет теория диффузии свободных медиаторов (напр., простагландинов) в глазу. Эту теорию также подтверждают данные относительно того, что ингибиторы циклооксигеназы (напр., индометацин, другие нестероидные противовоспалительные лекарства) уменьшают риск возникновения КМО. (Надо отметить, этот факт был зафиксирован только относительно возникновения КМО после хирургической травмы переднего сегмента в результате удаления катаракты).
Еще одна версия возникновения КМО подчеркивает роль механических факторов, таких как тракции макулы из-за нарушения нормального соединения между стекловидным телом и сетчаткой. Однако даже в соответствии с этой версией предполагается, что локальные силы натяжения провоцируют освобождение медиаторов, что и приводит к нарушению структуры гемато-ретинального барьера и, соответственно – возникновению КМО.
Световое повреждение, очевидно, также имеет место при развитии КМО после удаления катаракты, однако научно пока еще не подтверждено прямое влияние светового повреждения сетчатки на возникновение КМО.
Частота заболевания
Частота возникновения КМО по причинам, не связанным с хирургией катаракты, может варьировать в зависимости от этиологии или сопутствующего заболевания, на фоне которого возникает КМО. Разнобой в данных, которыми мы располагаем, происходит по разным причинам: с одной стороны, поскольку на ранних стадиях развития КМО еще клиническая картина почти незаметна, некоторые хирурги часто предпочитают ставить диагноз заболевания с целью не пропустить его; с другой стороны флюорисцентная ангиография (ФАГ) или оптическая томография глаза (ОСТ), которые могут помочь в точном определении КМО, делаются не всегда.
Среди мужского и женского населения КМЭ встречается одинаково часто.
Возраст возникновения КМО варьирует соответственно этиологии заболевания.
Клиническая картина заболевания
Пациенты с КМО обычно жалуются на не сопровождающуюся болезненными ощущениями потерю зрения в одном глазу. Однако, в зависимости от этиологии, потеря зрения может наблюдаться в обоих глазах и даже сопровождаться болезненными ощущениями. Симптомы обычно проявляются постепенно; однако часто пациенты обнаруживают их неожиданно при проверке глаз отдельно. КМО различного происхождения имеют разную клиническую картину. Наиболее часто встречающиеся случаи приводятся ниже.
Диабетическая макулопатия
Диабетическая макулопитая повреждает капилляры в районе макулы, что приводит к макулярному отёку. Иногда это приводит к развитию кистоидных изменений в районе фовелы. Чаще всего это встречается в случаях диффузного или хронического диабетического макулярного отёка, при этом зрение может ухудшиться до уровня 20/200.
При раннем лечении глаз с клинически явными проявлениями макулярного отёка (напр., когда отёк нарушает гомеостаз сетчатки, приводя к ее заметному утолщению) до наступления стадии диффузного отёка, возникновения КМО можно избежать, если пациент внимательно относится к своему здоровью и постоянно контролирует состояние своих глаз.
На фоне диабетического макулярного отёка КМО часто возникает при условии наличия адгезии задней гиалоидной мембраны и сетчатки, тогда как у пациентов с отделенной задней стенкой стекловидного тела КМО развивается намного реже. Наличие связи с задней стенкой стекловидного тела может быть причиной механического механизма развития КМО, при котором силы тракции приводят к формированию кистоидных полостей в макуле. В другом случае тракции макулы могут оттягивать сетчатку от помпы пигментного эпителия сетчатки (ПЭС). Иногда даже при отсутствии тракции задней стенки стекловидного тела существующая преретинальная мембрана может вызывать тяговые силы, что также приводит к развитию КМО.
Возрастная макулярная дегенерация
Возрастная макулярная дегенерация (ВМД) может проявляться в одной из двух форм: атрофической и экссудативной (сухой или влажной). Атрофическая макулярная дегенерация без экссудативных изменений обычно не приводит к развитию КМО. Экссудативная форма ВМД с хороидальной неоваскуляризацией может привести к серьезному отслоению лежащей сверху сетчатки и развитию КМО.
КМО чаще встречается при серозном отслоении макулы на протяжении 3-6 месяцев или в случае, если хороидальная неоваскулярная мембрана захватывает большую часть субфовеолярной области. В таких случаях вероятность реставрации хорошего зрения низкая.
Тромбоз сосудов сетчатки
Закупорка сосудов сетчатки, в частности тромбоз периферических сосудов сетчатки (ТПСС) или тромбоз центральных сосудов сетчатки (ТЦСС), может привести к развитию макулярного отёка в результате поражения капиллярного эндотелия на почве увеличенного гидростатического давления в сосудах. Сквозь стенки пораженных сосудов жидкость просачивается в межклеточное пространство, в результате чего можно видеть внутрисетчаточные кистоидные пространства. Эта форма КМО может вести к дальнейшей потере зрения, обычно постоянной, если такое состояние длится более 6 месяцев.
Макулярный отёк можно лечить, применив лазерную терапию (даже при сроках эдемы более 6 месяцев) или улучшив состояние соответствующих сосудов. Однако, если лазерная коагуляция улучшает зрение у пациентов с ТПСС, то у пациентов с ТЦСС после лечения макулярного отёка зрение не улучшается. В таких случаях даже при полном устранении отёка зрение остается таким же, как и до лечения.
Более современные методы лечения макулярного отёка на почве тромбоза сосудов сетчатки включают интравитреальное применение стероидов и ингибиторов факторов эндотелиального роста.
Эпиретинальные мембраны за счёт контрактуры мембраны могут приводить к сморщиванию лежащей под ними сетчатки. Иногда в таких случаях макулярный отёк может развиваться из-за искривления и растяжения окружающих сосудов внутри сетчатки. Если отёк не лечить, изменения архитектуры внутри сетчатки могут привести к образованию кистозных полостей. Эти изменения архитектуры могут происходить вследствие механической тракции, ведущих к отёку, или вследствие потери связи между сетчаткой и помпой пигментного эпителия сетчатки (ПЭС). В идеале хирургическое удаление разросшейся эпиретинальной мембраны, приведшей к ретинопатии сморщенной поверхности и макулярной эдеме с ухудшением зрения до уровня 20/80 – 20/100, необходимо произвести до того, как наступит необратимый КМО.
Хороидальные новообразования, такие как злокачественная меланома, невус или капиллярная гемангиома, могут так же приводить к КМО. Эти кистозные изменения могут происходить в слоях, лежащих над новообразованиями и в макуле, даже если новообразование находится на каком-то расстоянии от макулы. Этот феномен называют теорией макулярной акцентуации Вайса. Источником КМО на уровне капиллярной сети сетчатки являются изменения в мелких сосудах внутри сетчатки в виде разрастания клеток эндотелия.
При хроническом увеите, особенно pars planitis, также может развиваться КМО, скорее всего по причине нарушений барьера между кровеносной системой и сетчаткой. Хронические воспалительные процессы разрушают целостность перимакулярных кровеносных сосудов, приводя к образованию кистоидных полостей.
Другая картина, отличная от pars planitis, наблюдается при КМО, возникающем на фоне перифлебита сетчатки и при заднем витриите. Такие ситуации чаще возникают у женщин среднего возраста и имеют двухсторонний характер. Большая часть таких пациентов имеет относительно хорошее зрение на протяжении длительного периода времени.
Радиационная ретинопатия может по внешним признакам напоминать диабетическую ретинопатию. В таких случаях часто развивается форма макулярного отёка, очень напоминающая диабетический макулярный отёк.
Перифовеолярная телеангиэктазия сетчатки или заболевание Коатса характеризуется расширением и нарушением проницаемости сосудов сетчатки. Эти телеангиэктатические изменения могут проявляться на уровне артериол, венул или капилляров. Чем ближе поврежденные сосуды к макуле, тем быстрее начинают проявляться симптомы. Вследствие просачивания сквозь поврежденные сосуды сетчатки может проявляться клиническая картина КМО. Идиопатическая юкстафовеолярная телеангиэктазия является более мягкой формой телеангиэктазии, это заболевание характерно для височной части макулы, и оно имеет меньше шансов развиться в КМО.
КМО без просачивания при ФАГ обычно обнаруживается у мужчин среднего возраста, которые принимают большие дозы никотиновой кислоты для лечения гиперхолестеролемии.
Развитие КМО после успешной хирургической отслойки сетчатки обычно происходит у 30-43 % прооперированных в течение первых 4-6 недель после операции. В афакических глазах процент КМЭ может достигать 64 %. Большему риску развития КМО после хирургического лечения отслойки сетчатки подвергаются пациенты в старшем возрасте.
Частота возникновения КМО после кератопластики варьируется от 20 до 43 %. Афакические глаза подвергаются большему риску развития послеоперационного КМО. Если во время операции была проведена витректомия передней гиалоидной мембраны, то риск развития КМО возрастает в 8-9 раз.
Пигментный ретинит (ПР) также может сопровождаться КМО. Исследования показали, что в глазах с ПР очень высокая степень просачивания флюоресцеина через пигментный эпителий сетчатки (ПЭС) и перифовеолярные капилляры. Исследования выявили увеличенное количество циркулирующих антител к тканям сетчатки у пациентов с ПР и КМО. Это говорит в пользу гипотезы о возможном участии аутоиммунных процессов в развитии КМО у пациентов с ПР.
Хориоретинопатия Birdshot («след медведя») характеризуется большим количеством маленьких круглых и овальных пятнышек с недостаточной пигментацией на уровне хороидального слоя пигментного эпителия сетчатки (ПЭС). При этом часто наблюдается витриит, отек диска и просачивание флюоресцеина через сосуды сетчатки. Это заболевание также может сопровождаться развитием КМО.
Описаны случаи КМО при псевдоопухолях обриты, который исчезал после лечения орбитального заболевания.
Известны случаи развития КМО при лечении глаукомы препаратами простагландинового ряда – латанопростом. Существует мнение, что именно простагландиновый эффект латанопроста приводит к такому результату. Обычно после отмены препарата КМО исчезает. Очевидно, длительное применение латанопроста в некоторых случаях может приводить к возникновению васкулярной недостаточности барьера между сетчаткой и кровеносной системой глаз.
КМО также развивается у ВИЧ-инфицированных пациентов, у которых в сетчатке обнаружен цитомегаловирус (ЦМВР), а также у пациентов с пониженным иммунитетом. У некоторых пациентов КМО развивается на фоне излечения ЦМВР.
Наследственная форма КМО описана как макулярная дистрофия, проявляющаяся в среднем возрасте и постепенно прогрессирующая в последующие десятилетия. Исследования глаз с данной патологией показывают, что здесь изменения в основном происходят в внутреннем ядерном слое, так что такое заболевание может рассматриваться как первичное заболевание клеток Мюллера.
Фовеолярный первичный ретиношизис может быть ошибочно принято за КМЭ.
Дифференциальная диагностика
-
Тромбоз периферических сосудов сетчатки (ТПСС)
-
Тромбоз центральных сосудов сетчатки (ТЦСС)
-
Диабетический макулярный отёк
-
Макулярный отёк Ирвинга-Гасса
-
Увеит.
Дополнительные инструментальные исследования
Оптическая когерентная томография сетчатки является стандартным критерием при идентификации КМО. Она является неинвазивным способом получения изображения, которое позволяет определить наличие КМО через визуализацию заполненных жидкостью полостей в сетчатке. Можно также отслеживать развитие КМО на протяжении определенного периода времени, производя последовательные измерения размеров кистоидных полостей на срезах изображения макулы.
Исследования показали, что применение ОСТ более информативно, чем ФАГ, особенно если применяются новые томографические сканнеры с высокой степенью разрешения. Томография дает возможность измерения толщины сетчатки, а также количественных изменений макулярного отёка с течением времени. Этот неинвазивный метод особенно хорош при отслеживании течения процесса лечения глаз.
Новое программное обеспечение для глазных томографов увеличило их возможности до идентификации особых разновидностей КМО. Спектрально доминантные томографы увеличили разрешающие возможности томографического изображения до 2-3 микрон, что сделало их ещё более чувствительными.

ОСТ кистоидного макулярного отёка у пациента, страдающего увеитом.
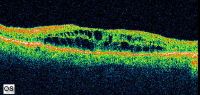
Томографическое изображение кистоидного макулярного отёка в глазу с непролиферативной диабетической ретинопатией.
ФАГ является альтернативным методом выявления КМО.
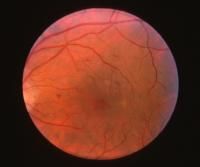
Фотография глазного дна пациента с непролиферативной диабетической ретинопатией, где четко офтальмоскопируется клинически явный макулярный отёк.
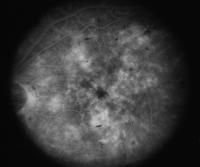
Ангиограмма того же глаза, на которой виден КМО и просачивания из микроаневризм, характерные для диабетической ретинопатии.
Сосудистые коллатерали, пересекающие горизонтальную линию на ФАГ, могут помочь выявить, что причина отёка (а также кровоизлияний в сетчатке, если они есть), скорее всего, в закупоривании сосудов.
Отсутствие ликиджа на ФАГ позволяет поставить диагноз токсической ретинопатии и юношеского фовеолярного ретиношизиса.
Амбулаторное лечение
Существует несколько методов лечения неартифакического КМО в зависимости от причины возникновения эдемы / заболевания.
В случаях возникновения КМО на фоне медикаментозной терапии, такой как применение латанопроста или никотиновой кислоты, прекращения применения препаратов обычно достаточно для исчезновения проявлений КМО.
Стероиды местного применения и нестероидные противовоспалительные препараты используются для лечения КМО, особенно в случаях, когда КМО возникает на фоне увеита. Большинство исследований посвящено изучению применения этих препаратов для лечения артифакического КМО после хирургического удаления катаракты. Однако эффект данных медикаментов относительно стабилизации гемато-ретинального барьера может быть использованным также для лечения и других форм КМЭ.
Инъекции стероидов пролонгированного действия (напр., триамцинолон) в субтеноновое пространство обычно более эффективны и используются для лечения неинфекционного увеита.
Такие инъекции более эффективны, чем парабульбарное введение и более безопасны с точки зрения опасности травмы глаза.
Инъекции триамсиналона дают очень хороший эффект при лечении КМО в глазах с разными видами осложнений, включая артифакическую КМО, тромбоз сосудов сетчатки, диабетический макулярный отёк, увеит и юкстафовеальную телеангиэктазию. В данный момент проводятся клинические испытания относительно длительности достигаемого результата и безопасности данного вида лечения.
Исследования показали, что факторы роста эндотелия сосудов (VEGF) являются важными медиаторами проницаемости сосудов и КМО. Поэтому сейчас проводятся также клинические испытания относительно оценки положительного эффекта ингибиторов VEGF при лечении КМО при таких заболеваниях, как диабетический макулярный отёк и тромбоз центральных сосудов сетчатки.
Стероиды орального применения также являются обычными препаратами, используемыми для стабилизации барьера между сетчаткой и кровеносной системой глаза при лечении воспалительных процессах в глазу и КМО у пациентов с задними и средними увеитами.
Однако применения оральных стероидов следует избегать, если в этом нет настоятельной необходимости, поскольку их систематическое применение может привести к осложнениям общего характера.
При возникновении КМО на фоне диабетической ретинопатии, согласно руководству Исследования Раннего Лечения Диабетической Ретинопатии (ИРЛДР), необходимо провести фокальную лазерную фотокоагуляцию.
Однако, возникающий на фоне диабета диабетический макулярный отёк, часто переходит в хроническую форму и не поддается адекватно лазерному лечению. Некоторые специалисты для лечения диабетической макулярной эдемы, рекомендуют провести субтеноновые инъекции триамцинолона или внутрь глаза параллельно с макулярной лазерной фотокоагуляцией или без нее.
КМО на фоне хороидальной неоваскуляризации при влажной форме возрастной макулодистрофии является вторичной реакцией на наличие субретинальной неоваскуляризации.
Макулярный отёк часто является причиной потери зрения в глазах с тромбозом центральной вены сетчатки либо ветви центральной вены сетчатки.
Макулярная лазерная фотокоагуляция дает хорошие результаты, улучшая зрение у пациентов с тромбозом ветви центральной вены сетчатки (при остроте зрения 20/40 или меньше). Однако, исследования не показали положительных результатов при лечении тромбоза центральной вены сетчатки.
Инъекции триамциколона внутрь стекловидного тела считаются эффективными при лечении КМО у пациентов с тромбозом ветви ЦВС и в какой-то мере при неишемической форме тромбоза ЦВС.
КМО, возникший на фоне других причин, лечится соответственно данных причин заболевания. КМО, возникший на фоне цитомегаловируса ретинитис (ЦМВР), лечится с применением специальной противовирусной терапии (напр., ганцикловир, фоскарнет, цидофовир).
КМЭ, возникшая на фоне юкстафовеолярной телеангиэктазии при заболевании Коатса, хорошо поддается лазерной фотокоагуляции. При этом также улучшается зрение.
Орбитальные псевдоопухоли хорошо поддаются лечению стероидами орального применения. В случаях, где кроме орбитального псевдоновообразования присутствует также КМО, он попутно исчезает при лечении ведущего заболевания.
Другие формы КМО хорошо поддаются лечению ацетазоламидом (диакарб). К таким относятся КМО, образовавшиеся после склерального пломбирования, на фоне некоторых форм увеита, а также КМО на фоне пигментной дегенерации сетчатки или пигментного ретинита.
Хирургические методы решения проблемы
КМО не относится к заболеваниям, которые лечатся хирургическим путем. Однако осложнения, возникшие на фоне КМО в глазу, могут потребовать хирургического вмешательства.
Наличие эпиретинальной мембраны может способствовать возникновению и развитию ретинопатии сморщенной поверхности и КМО. Хирургического удаления эпиретинальной мембраны часто может быть достаточно для излечения КМО и улучшения зрения.
Причиной синдрома витреомакулярного натяжения является тракция макулы стекловидным телом. Одним из его симптомов является КМО. При таких условиях устранение растяжения витректомическим способом часто может иметь результатом устранение макулярной эдемы.
В случаях возникновения КМО на фоне заболевания Коатса или периферического увеита применение криотерапии к периферическим зонам экссудации может способствовать исчезновению жидкости и в кистоидных полостях макулы.
Медикаменты, рекомендуемые для лечения КМО
В число медикаментов, наиболее часто используемых для лечения КМО, входят стероиды, нестероидные противовоспалительные препараты (НПП) и ацетазоламид.
Ингибитор фактора роста васкулярного эндотелия
Ингибитор фактора роста васкулярного эндотелия является мощным медиатором ангиогенезиса и проницаемости сосудов.
Обычно пациенты с КМО находятся под наблюдением у специалиста на протяжении 1-3 месяцев с целью наблюдения за эффективностью лечения.
Возможные осложнения
Осложнения при лечении КМО возникают нечасто. После инъекций триамцинолона в субтеноновую зону пациенты могут иногда испытывать кратковременное ослабление мышцы верхнего века или субконьюнктивное кровоизлияние.
Интравитреальные инъекции триамцинолона могут приводить к осложнениям в виде увеличения внутриглазного давления, прогрессированию развития катаракты, разрывам или отслоению сетчатки, инфекционному и неинфекционному эндофтальмиту, а также механическому повреждению хрусталика.
Прогнозы
Прогноз изменений остроты зрения в глазах с КМО зависит от этиологии отёка. Если КМО поддается лечению, острота зрения, как правило, возвращается к состоянию 20/40 или лучше. Однако, в застарелых случаях КМО, зрение часто не поднимается выше 20/100 или 20/200.







Коментарі
Завантаження...