Альтернативные виды и формы лечения Анти-VEGF при экссудативном изменении сетчатки, вызванном возрастной макулярной дистрофией
(современное состояние вопроса)
Автор изображения: Holger Lippmann.
Краткий обзор
Использование разнообразных форм и методов лечения неоваскулярной пролиферации, связанных с применением инъекций и комбинированной терапии, возникло как альтернатива общепринятой монотерапии ингибиторами ангиогенеза, которая связана с необходимостью ежемесячного применения препаратов и связанных с этим финансовых затрат для пациентов, рисков и побочных эффектов, а также уровнем рабочей нагрузки лечебных учреждений.
Лечение с помощью анти-VEGF препаратов требуют чёткого графика их применения. Хотя большинство данных, полученных в результате не системно проводимых экспериментов, в основном демонстрируют менее многообещающие результаты непостоянных форм и методов лечения VEGF, положительные результаты некоторых исследований склоняются в пользу применения разнообразных режимов введения препаратов.
Очевидность необходимости комбинированного лечения будет зависеть от результатов рандомизированных клинических исследований, сравнения результатов альтернативных форм и режимов лечения с результатами, полученными от использования стандартной ежемесячной в течение 24 месяцев anti-VEGF монотерапии.
С тех пор, как использование анти-VEGF лечения стало доступным для лечения экссудативных изменений сетчатки, вызванных возрастной макулярной дегенерацией (AMD), офтальмологами постоянно обсуждаются и пересматриваются стандарты лечения.
Обобщая данные альтернативных форм и методов лечения анти-VEGF, их можно классифицировать следующим образом:
• лечение в виде монотерапии с режимом инъекций не чаще одного раза в месяц и продолжительностью лечения – 1-2 года;
• комбинированное терапевтическое лечение, при котором анти-VEGF препараты сочетаются с другими препаратами, в частности введение в стекловидное тело кортикостероидов и проведения вертепорфино-фотодинамической терапии.
При использовании альтернативных терапевтических режимов лечения перед врачами стоят несколько задач:
- Прежде всего, уменьшить количество и частоту инъекций, тем самым сокращая риски, связанные как с введением препарата в стекловидное тело, так и с использованием самих лекарственных препаратов, а так же сократить затраты по лечению;
- Определить сроки лечения после прекращения активной фазы заболевания, тем самым определяя конечную точку терапевтического лечения;
- Добиться видимого улучшения результатов в сравнении с результатами применяемой стандартной терапии за счёт достижения аддитивного (полученного за счёт положительного эффекта последовательно применяемых методов) либо синергического (при применении совместно нескольких методов лечения) эффекта.
В основе оценки альтернативных режимов лечения лежит наблюдение пациентов в клинических условиях и определение терапевтического эффекта, эквивалентного тому, который достигается при использовании стандартного ежемесячного лечения препаратом Ранибизумаб (торговое наименование Луцентис) при лечения возрастной макулодистрофии (ВМД), определённого в ходе исследований MARINA и ANCHOR. В этой статье оценивается относительная эффективность текущих альтернативных анти-VEGF методов лечения неоваскулярной ВМД на основе имеющихся доклинических и клинических данных, а также продолжающихся клинических исследований.
Современные терапевтические методы лечения экссудативной ВМД.
В настоящее время для лечения экссудативной ВМД используются пять видов фармакологической терапии (рис. 1).
Три вида терапии одобрены FDA США (Управление по контролю за продуктами и лекарствами) с показаниями для применения следующих медицинских препаратов: вертепорфин фотодинамическая терапия, Macugen (Eyetech фармацевтика, Нью-Йорк, США) и ранибизумаб (Луцентис ®; Genentech, Inc., США).
Интравитреальные инъекции бевацизумаба (Авастин ®;. Genentech, Inc) и триамцинолона ацетонид также широко используются для лечения экссудативной ВМД.
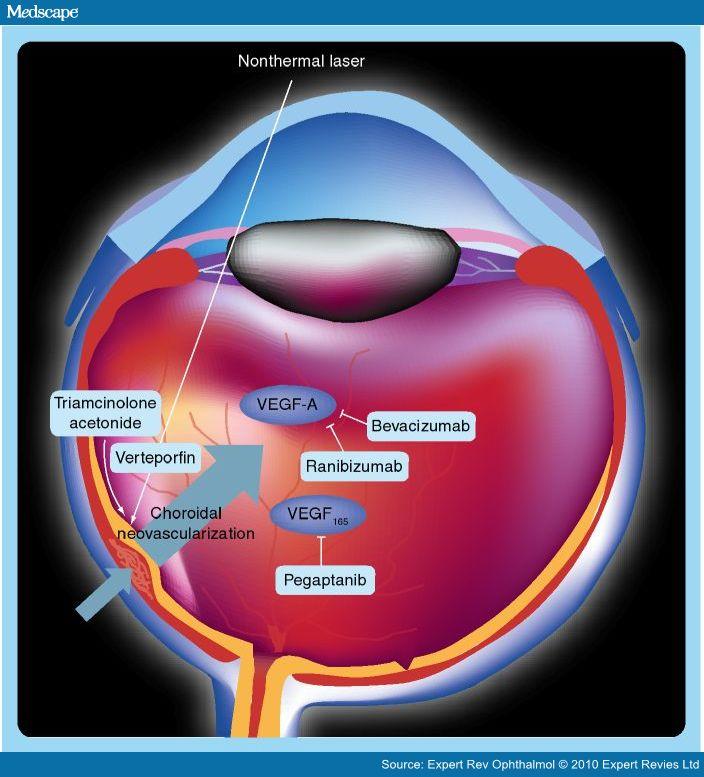
Рисунок 1. Механизмы воздействия, используемые сегодня в терапии лечения экссудативной возрастной макулодистрофии.
В настоящее время для лечения экссудативной возрастной макулодистрофии используются пять видов препаратов: вертепорфин для фотодинамической терапии, анти-VEGF аптамер pegaptanib натрия, ориентированный на VEGF165, и анти-VEGF-моноклональных антител ранибизумаб, который предназначен для всех изоформ VEGF и продуктов его разложения. Терапевтические методы, используемые не по инструкции, относящейся к применению лекарственных препаратов для лечения заболеваний, и не указанные в инструкции, утверждённой Администрацией по контролю за лекарствами и медицинскими препаратами, включают кортикостероидные ацетонид триамцинолона и анти-VEGF гуманизированные моноклональные антитела бевацизумаба.
В настоящее время ранибизумаб и бевацизумаба наиболее широко используются в лечении неоваскулярной ВМД. Ранибизумаб является препаратом для лечения возрастной макулодистрофии (ВМД). Он связывает все VEGF-изоформы с их биологически активными продуктами распада. Бевацизумаб получен из той же молекулы, что молекула-родитель ранибизумаб. Это гуманизированное VEGF-антитело, которое также связывает все VEGF-изоформы и их биологически активные продукты распада. Хотя бевацизумаб одобрен FDA только для внутривенного применения в комбинированном лечении с применением химиотерапии для лечения колоректального рака, молочной железы, лёгких и почек, клинический опыт применения бевацизумаба показал, что этот препарат хорошо переносится организмом и способствует улучшению зрения и снижению толщины сетчатки у больных с экссудативной ВМД.
С учётом стоимости, которая существенно ниже, чем стоимость препарата ранибизумаб, бевацизумаб приобрёл большую популярность, как препарат AMD, относящийся к лекарствам для лечения заболеваний, не указанных в инструкции, утверждённой Администрацией по контролю за продуктами питания и лекарствами.
Развитие терапии.
В дополнение к вышеупомянутым видам терапевтического лечения в настоящее время используется несколько методов лечения. В стадии клинической разработки для лечения экссудативной ВМД, в том числе VEGF «приманка рецептор» Trap-Eye (Regeneron, Нью-Йорк, США), радиоизотопные Epi-Rad90 ™ Офтальмология System (NeoVista, Inc, штат Калифорния, США), siRNAs, таких как bevasiranib (OPKO Health, Inc, штат Флорида, США), миРНК-027 (Therapeutics, Колорадо, США) и PDGF ориентированный аптамер E10030 (Ophthotech корпорации , Нью-Джерси, США). Многие из этих новых препаратов находятся на стадии прохождения исследований и экспериментов в той или иной форме комбинированной терапии для определения стратегии развития их дальнейшего применения, либо в качестве дополнительной терапии (интегрированной с анти-VEGF-препаратами) или в качестве последующего (техническое обслуживание) лечения после первоначального лечения ранибизумабом.
Обоснование целесообразности режимов переменного дозирования
В клинической практике сегодня лишь немногие специалисты в области изучения лечения сетчатки глаза придерживаются строгого графика регулярных, в течение 2 лет, ежемесячных интравитреальных инъекций, установленных исследованиями MARINA и ANCHOR. Появились и появляются различные постоянно меняющиеся стратегии лечения, в большинстве из которых на начальной стадии используются несколько ежемесячных инъекций, затем каждая новая инъекция сопровождается фиксированным прерывистым графиком (например, каждые 3 месяца) или по мере необходимости (PRN-pro re nata). Хотя главным, что принимается во внимание в снижении частоты дозирования, является стоимость препарата, режим переменного дозирования в процессе лечения преобладает даже при использовании такого препарата, более низкого по стоимости, как бевацизумаб.
В основе аберрантной (переменной) терапии, лежит принцип избежать лечения, в том случае, когда это не считается необходимым, а именно – когда после лечения макула становится «клинически сухой».
Снижение частоты инъекций при достижении эквивалентных результатов ставит своей целью повысить терапевтическую эффективность. В ходе диспансерного наблюдения пациентов в графиках-схемах PRN или прерывистого лечения фиксируются состояние пациента и регистрируются моменты появление экссудата.
В основе такого подхода лежит индивидуальный подход к лечению пациента, где акцент делается на мнение лечащего врача по отношению к каждому отдельно взятому пациенту и организации его лечения.
С другой стороны, рациональность научного обоснования для стандартного непрерывного ежемесячного терапевтического лечения основана на данных VEGF биологии, фармакокинетике препарата и данных III фазы клинических исследований.
VEGF постоянно появляется в изменённых сетчатке и пигментном эпителии сетчатки (ПЭС). В исследованиях, проведенных на взрослых приматах и грызунах, наблюдалась повторяющаяся выработка VEGF в неоваскулярной мембране хориоидеи. Что кается людей, то доказательством того, что при экссудативной форме ВМД процесс продукции VEGF поддерживается постоянно, является то, что даже в отдалённые сроки после хирургического удаления неоваскулярной мембраны определялся высокий уровень экссудативный VEGF.
Доказательством того, что необходимо ежемесячное введения анти-VEGF являются фармакокинетические данные по использованию ранибизумаба и бевацизумаба. Препараты относятся к крупномолекулярным биопрепаратам, которые быстро разлагаются и выводятся из глаза.
В стекловидном теле глаз кроликов и приматов 0,5 мг ранибизумаба имеет период полураспада 2,9 и 2,6 дня соответственно. Для человеческих глаз, период полураспада составляет около 3 дней, с допустимым отклонением от положенного значения величины ниже эффективных концентраций в течение 4 недель. Для препарата бевацизумаб, фармакокинетические данные показывают, что в стекловидном теле глаза кролика полураспад этого препарата составляет около 4 дней, а в стекловидном теле человеческого глаза полураспад этого препарата составляет 6,7 дней.
Данные клинических исследований
Стандартные дозировки.
На основе клинических испытаний III уровня, проведенных двумя компаниями MARINA и ANCHOR, был определён непрерывный режим и дозы ежемесячных инъекций.
В обоих клинических испытаниях, из обследованных MARINA 716 пациентов с минимально классически выраженной, а также латентной хориоидальной неоваскуляризацией, и 423 пациентов с преимущественно классическими проявлениями хориоидальной неоваскуляризацией (ХНВ), обследованных компанией ANCHOR, в группе лечения с применением препарата ранибизумаб, пациенты получали в течение 2 лет ежемесячные интравитреальные инъекции (0,3 или 0,5 мг).
Через 12 месяцев, у пациентов MARINA наблюдалось повышение остроты зрения на 6,5 и 7,2 знака. В ANCHOR за 12 месяцев пациенты показали в среднем увеличение остроты зрения на, соответственно, 8,5 и 11,3 знака. За аналогичный промежуток времени у пациентов, которые принимали препарат не систематически и не регулярно, отмечалось снижение зрения в среднем на 9,5 знака.
И в MARINA и в ANCHOR улучшение зрения продолжалось в течение 24 месяцев: в этот период пациенты MARINA, которые принимали препарат ранибизумаб в дозировке 0,3 и 0,5 мг, показали увеличение остроты зрения на 5,4 и 6,6 знака соответственно, в группе пациентов, которые принимали препарат не регулярно, наблюдалось снижение остроты зрения на 14,9 знака. Пациентами ANCHOR, строго принимавшими препарат ранибизумаб в 0,3 и 0,5 мг, достигнуто среднее увеличение остроты зрения на 8,1 и 10,7 знака, соответственно, по сравнению со снижением остроты зрения на 9,8 знака у пациентов, которые принимали вертепорфин (ФДТ).
Переменное дозирование
Шестью клиническими исследованиями – PIER, PRONTO, SUSTAIN, HORIZON, EXCITE и SAILOR была доказана безопасность и эффективность используемой схемы лечения ранибизумабом в монотерапии (у пациентов с субфовеальной хориоидальной неоваскуляризацией на фоне возрастной макулодистрофии, вторичным отёком макулы). В то время как в исследованиях, проводимых компаниями PIER и EXCITE, использовался переменный режим с фиксированными интервалами времени приёма препарата, в исследованиях PRONTO, HORIZON, SUSTAIN и SAILOR использовался PRN (pro re nata – по мере необходимости) режим.
В PIER исследованиях (фаза III) препарат назначался в виде инъекций с использованием фиксировано переменного протокола инъекций, в котором ВМД пациенты (n = 184) с классической неоваскулярной мембраной получали ранибизумаб в дозировке (0,3 или 0,5 мг) или плацебо в течение первых 3 месяцев, после чего курс инъекций повторялся каждые 3 месяца. Данный альтернативный режим дозирования был выбран на основе проведенных ранее исследований фазы I и II, которые показали, что клинический эффект применения препарата ранибизумаб в дозировке (0,3 и 0,5 мг) может длиться в течение 90 дней.
Во время применения ежемесячных инъекций, пациенты, получавшие ранибизумаб, показали увеличение остроты зрения к третьему месяцу с момента начала приёма препарата.
Тем не менее, в течение последующих месяцев, когда инъекции делались регулярно каждые три месяца, наблюдаемое у пациентов ранее улучшение остроты зрения остановилось, а в дальнейшем острота зрения снизилась на 1,6 и 0,2 знака у пациентов в группах, которые принимали препарат ранибизумаб в дозировке 0,3 и 0,5 мг, соответственно.
В группе пациентов, принимавших плацебо, острота зрения ухудшилась на 16,3 знака.
Результаты длившихся в течение 2 лет открытых исследований I и II фаз, проведенных при финансовой поддержке PrONTO (количество пациентов 40), оказали большое влияние на то, что режимы PRN нашли широкое применение в клинической практике. В основе режима PrONTO лежит использование инъекций ранибизумаб в дозировке (0,5 мг) в течение 3-месяцев, с последующим ежемесячным селективным дозированием. Установлены строгие критерии, предъявляемые к обоснованию необходимости повторения инъекции, а именно: ухудшения остроты зрения на пять и более знаков в сочетании с данными оптической когерентной томографии – появление зон отёка и утолщения центральной сетчатки на 100 и более микрон, а так же рецидив макулярной геморрагии.
Полученные в течение года данные показали, что в результате применения, предложенного PrONTO режима лечения, количество инъекций в среднем уменьшилось в 5,6 раз в течение первого года лечения. При этом улучшение остроты зрения в среднем по сравнению с исходными данными составило 9,3 знака. В течение 2-х лет, среднее число инъекций составило 9,9, а улучшение остроты зрения составило в среднем 11,1 знака.
Проведенное SAILOR исследование является на сегодня самым крупным исследованием уровня фазы III-b экссудативной ВМД (количество пациентов 4307, сроки наблюдение – 1 год). Ранибизумаб применялся в дозировке 0,3 или 0,5 мг на протяжении 3-х месяцев с последующим PRN дозированием в двух группах пациентов. В дальнейшем, диспансерное наблюдение осуществлялось через каждые 3 месяца, а критерием проведения повторной инъекции было ухудшение остроты зрения на более чем пять знаков, по сравнению с максимальной остротой зрения пациента, и/или утолщение сетчатки в макулярной области (по данным ОСТ) на более чем 100 микрон.
Среди пациентов (в количестве 2378 человек), которые наблюдались в течение 1 года и впервые получали лечение ранибизумабом в дозировке 0,3 и 0,5 мл, наблюдалось улучшение остроты зрения соответственно на 0,5 и 2,3 знака, а в группе пациентов, которые принимали препарат повторно, соответственно, на 1,7 и 2,3 знака. Результаты исследования SAILOR имеют расхождения с результатами исследований MARINA и ANCHOR.
Исследования, проведенные HORIZON (600 пациентов) явили собой своего рода продолжение цикла исследований, и дают другую оценку эффективности PRN терапии. Лечение по программе HORIZON проводилось в режиме PRN.
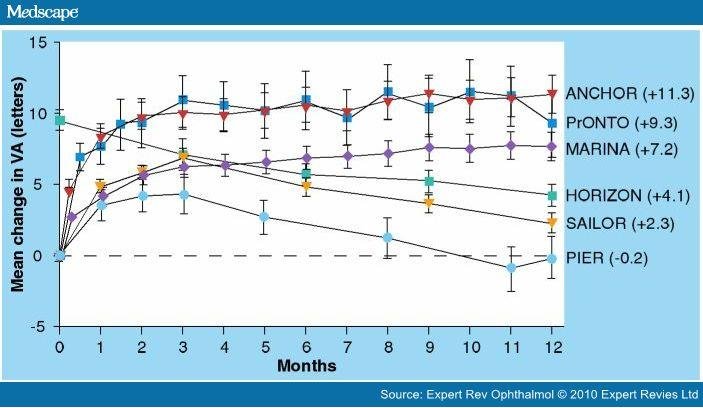
Сравнение средних изменений уровня остроты зрения в течение 12 месяцев у пациентов, принимавших препарат ранибизумаб в дозировке 0,5 мг, как стандартную терапию, так и переменную терапию, показано на рисунке 2.
Рисунок 2. Изменение остроты зрения при приёме ранибизумаба.
Средние значения потери либо прибавки количества знаков в процессе 12-месячного наблюдения при применении 0.5мг ранибизумаба при ежемесячном режиме ETDRS, ANCHOR, MARINA или в режиме по необходимости – PRN – HORIZON, SAILOR, PIER, PrONTO.
EXCITE исследование (фаза III-b) анализировало результаты лечения группы пациентов, которые принимали препарат ранибизумаб в дозах 0,3 или 0,5 мг в течение 3 месяцев, за которым последовало применение инъекций по принципу PRN, и группы пациентов, которые сразу получали лечение по принципу PRN. Предварительные данные свидетельствуют о большей эффективности лечения в группе пациентов, которые принимали лечение 3 месяца подряд с последующим индивидуальным режимом (PRN – инъекция по необходимости). Аналогичные данные были получены и в исследовании SUSTAIN (клинических испытаний фазы III-b), где пациенты в течение трёх месяцев получали препарат ранибизумаб в дозировке 0,3 мг, а затем в режиме PRN, которые определялись в зависимости от изменений остроты зрения пациентов.
Комбинированная терапия
Рациональность.
Поскольку имеющиеся методы лечения экссудативной ВМД предполагают различные механизмы воздействия, сочетания разных видов лечения могут обеспечить синергетический эффект.
В применении комбинированной терапии рациональным также является индивидуальное лечение – недостаточная реакция отдельного пациента на какое-либо лечение может быть решена за счёт перехода к другим, альтернативным методам.
Прекращение формирования НВМ является целью комбинированной терапии. Кроме того, в сравнении с применением монотерапевтического лечения, комбинированная терапия направлена на снижение частоты лечения, снижение сопутствующих рисков и уменьшение финансовых расходов.
Данные научно обоснованного сравнения анти-VEGF монотерапии и комбинированного лечение в настоящее время ограничены. Данные, описывающие результаты комбинированной терапии с применением VEGF препаратов в сочетании с PDT вертепорфина и/или внутриглазных кортикостероидов представлены недостаточно полно.
Требуются более длительные и стандартизированные исследования в этом направлении.
PDT плюс анти-VEGF-терапия
Программа FOCUS явилась 2-летним, рандомизированным, контролируемым исследованием уровня I / II фазы, в котором пациенты (количество 162) получали лечение с использованием фотодинамической терапии (PDT) в сочетании с ежемесячным интравитреальным введением препарата ранибизумаб дозировкой (0,5 мг) либо инъекции плацебо. Применение PDT использовалось за 7 дней до начала приёма препарата ранибизумаб, а затем по мере необходимости один раз в три месяца (что соответствует установленным стандартам). В течение последующих 24 месяцев наблюдения, пациенты получали лечение с помощью препарата ранибизумаб плюс PDT. Достигнуто повышение остроты зрения на 4,6 знаков по сравнению с пациентами, получавшими плацебо плюс PDT, у которых наблюдалось снижение остроты зрения на 7,8 знака.
В ряде случаев, комбинированная терапия с применением вертепорфина PDT и препарата бевацизумаб, как сообщается, способствовала улучшению уровня остроты зрения и уменьшению центральной толщины макулы у пациентов с экссудативной ВМД при одновременном сокращении повторных курсов лечения.
Рандомизированные исследования на предмет сравнения анти-VEGF монотерапии и комбинированной PDT терапии ещё предстоит провести. Продолжаются исследования (DENALI и MONT BLANC) по проведению фотодинамической терапии с применением вертепорфина в сочетании с препаратом ранибизумаб у пациентов с субфовеальной хориоидальной неоваскуляризацией, обусловленной возрастной макулярной дегенерацией.
Интравитреальные кортикостероиды плюс анти-VEGF-терапия
Ретроспективный анализ 30 пациентов, получавших интравитреально бевацизумаб и триамцинолон, показал, что у 27 из них наблюдалось улучшение остроты зрения со средним уменьшением толщины фовеалы на 164 микрон в течение первых 4 недель наблюдения.
Тройная терапия
Термин «Тройная терапия» относится к комбинированной терапии с применением анти-VEGF препаратов, интравитреальных кортикостероидов и PDT.
По итогам 40 недель наблюдений у 104 пациентов с экссудативной ВМД, применение тройной терапии с использованием препарата бевацизумаб вместе с PDT вертепорфином и интравитреальным дексаметазоном привело к улучшению остроты зрения на 1,8 знака и уменьшению толщины макулы на 182 микрон (р<0,01). Большинство пациентов прошли только один цикл лечения.
Обсуждение
Альтернативные схемы анти-VEGF-терапии для неоваскулярной ВМД, в частности переменный и PRN (pro re nata – по мере необходимости) режимы лечения, получили де-факто практическое клиническое применение. В основе этого абсолютная уверенность в терапевтической эквивалентности альтернативной анти-VEGF-терапии стандартной ежемесячной монотерапии. До сих пор, однако, в опубликованных докладах по результатам масштабных, многоцентровых рандомизированных исследований (PIER, SAILOR and HORIZON), PRN терапия показала не столь обнадёживающие результаты.
Предварительные данные открытого исследования, проводимого SUSTAIN, показали некоторые преимущества PRN режима, следующего за 3-месячным прерывистым режимом применения препаратов.
Каждое из этих исследований было ограничено временными рамками, нерегулярностью наблюдения за пациентом, графиками дозирования препаратов и не стандартизированными критериями повторного лечения, что привело к тому, что данные исследований в некоторых случаях противоречивы.
В конечном счёте, потребуется ещё не одно сравнение результатов режимов переменной, pro re nata и стандартной ежемесячной терапии. Такое исследование, в частности, сейчас проводит программа CATT.
Комментарий экспертов
Применение анти-VEGF-терапии привело к большому прорыву в лечении пациентов с экссудативной ВМД, создавая поле для широкого спектра терапевтических стратегий. В последние годы врачи приняли переменную и pro re nata схемы снижения частоты инъекций и комбинированные схемы использования анти-VEGFметодов лечения с одним или несколькими видами адъювантной терапии. Основная цель новых подходов в лечении – сбалансировать риски для пациента, финансовые расходы и затраты, связанные с применением ежемесячной VEGF-терапии. Что касается результатов исследования в пользу переменной, pro re nata или комбинированных подходов, единого мнения по этому вопросу пока нет.
Выводы, которые можно сделать на основе результатов масштабных рандомизированных исследований, говорящих о менее благоприятных терапевтических результатах при помощи pro re nata схем использования ранибизумаб, не являются объективными, поскольку данные исследования были ограничены протоколами и в них отсутствовали прямые сравнения с традиционными видами ежемесячного лечения. С другой стороны, убедительных доказательств в поддержку переменной и pro re nata схем лечения и комбинированной терапии добиться не удалось.
Ожидаемые результаты нескольких текущих клинических исследований должны обеспечить более высокий уровень достоверности данных для сравнения различных тактик лечения.
В частности, прямое сравнение pro re nata терапии с ежемесячной терапией будет проведено в исследованиях CATT. В ближайшее время будут получены результаты по сравнительной оценке применения препаратов ранибизумаб и бевацизумаб. Всё это будет иметь серьёзные последствия для клинической практики и позволит улучшить результаты лечения пациентов с экссудативной ВМД.
Общий обзор за пять лет
Применение анти-VEGF препаратов в значительной степени способствовало повышению качества оказания медицинских услуг при лечении пациентов с экссудативной ВМД. В настоящее время широко применяется разнообразный спектр терапевтических подходов и методов лечения. Результаты, которые в течение ближайших нескольких лет ожидаются от основных рандомизированных клинических исследований, будут способствовать систематизации передового опыта в отношении оптимальной частоты приёма препаратов, длительности режима лечения, а также роли комбинированной терапии.
Развитие новых методов лечения может привести к тому, что новые анти-VEGF технологии и лекарственные препараты станут более доступными. Расширение форм и методов лечения пациентов будет способствовать получению более высоких результатов терапевтической эффективности. В свою очередь это потребует новых клинических исследований, сравнительно-сопоставительного анализа на предмет определения эффективности новых форм, методов и технологий лечения.

Автор изображения: Magda







Коментарі
Завантаження...